- Головна
- Готові шкільні презентації
- Презентація на тему «Електричний струм у розчинах і розплавах електролітів» (варіант 1)
Презентація на тему «Електричний струм у розчинах і розплавах електролітів» (варіант 1)
258
Поділитись підручником в соціальних мережах
Слайд #1
Електричний струм у розчинах і розплавах електролітів. Закони електролізу. Застосування електролізу.

Слайд #2
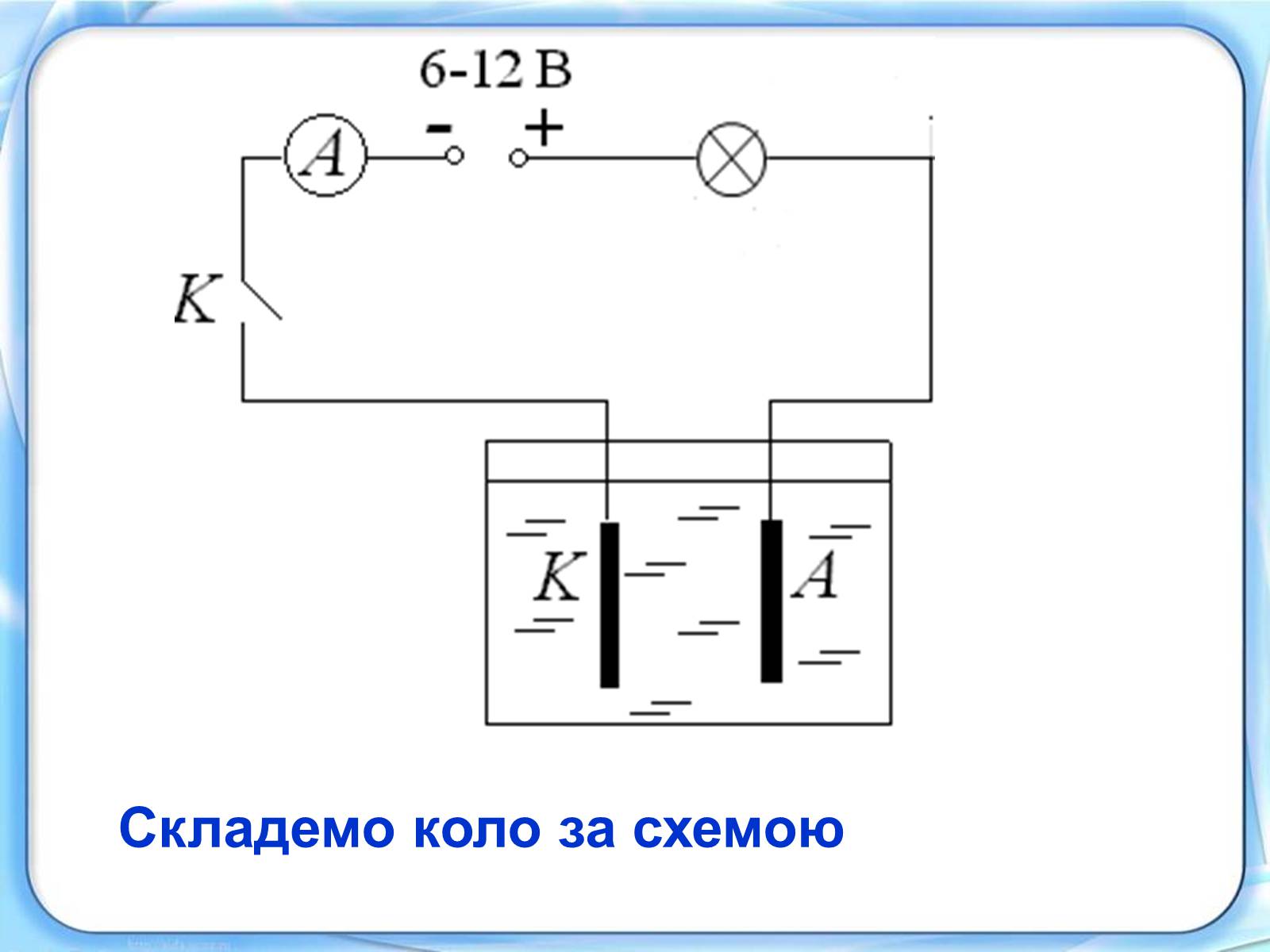
Складемо коло за схемою
Слайд #3
До провідників належать розплави і розчини електролітів: кислот, лугів і солей. Рідкими напівпровідниками є розплавлений селен, розплави сульфідів та ін.
Під час розчинення електролітів під впливом електричного поля полярних молекул води відбувається розпад молекул електролітів на іони. Цей процес називають електролітичною дисоціацією, в результаті якої нейтральні молекули розпадаються на позитивні та негативні іони. В електроліті з'являються вільні носії зарядів і він починає проводити струм.
Під час розчинення електролітів під впливом електричного поля полярних молекул води відбувається розпад молекул електролітів на іони. Цей процес називають електролітичною дисоціацією, в результаті якої нейтральні молекули розпадаються на позитивні та негативні іони. В електроліті з'являються вільні носії зарядів і він починає проводити струм.

Слайд #4
Оскільки заряд у водних розчинах чи розплавах електролітів переноситься іонами, то таку провідність називають іонною. За іонної провідності проходження струму пов'язано із перенесенням речовини. На електродах відбувається виділення речовин, які входять до складу електроліту. На аноді негативно заряджені частинки віддають свої зайві електрони (окиснювальна реакція), а на катоді позитивні іони отримують електрони (реакція відновлення).

Слайд #5
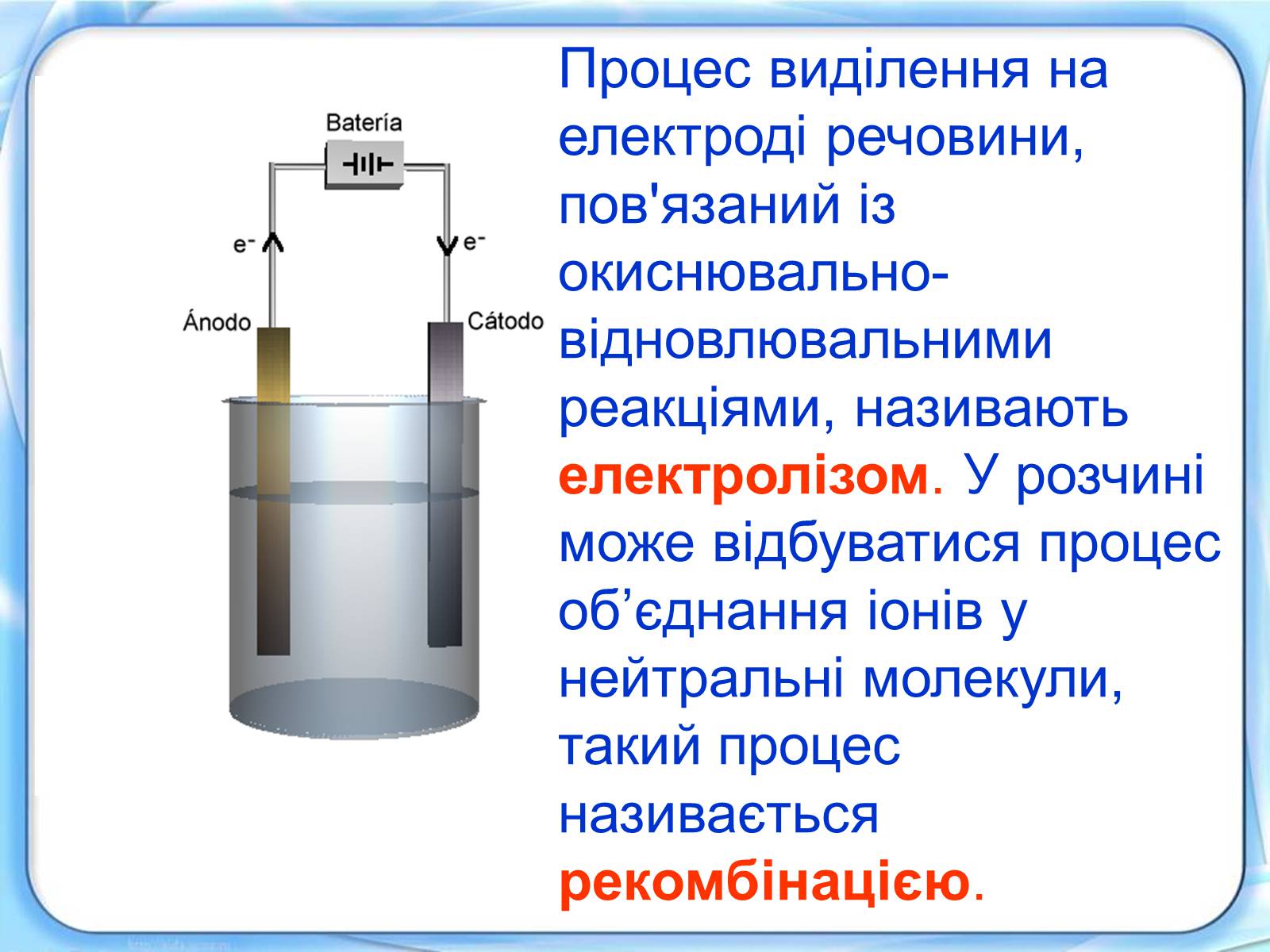
Процес виділення на електроді речовини, пов'язаний із окиснювально-відновлювальними реакціями, називають електролізом. У розчині може відбуватися процес об'єднання іонів у нейтральні молекули, такий процес називається рекомбінацією.
Слайд #6
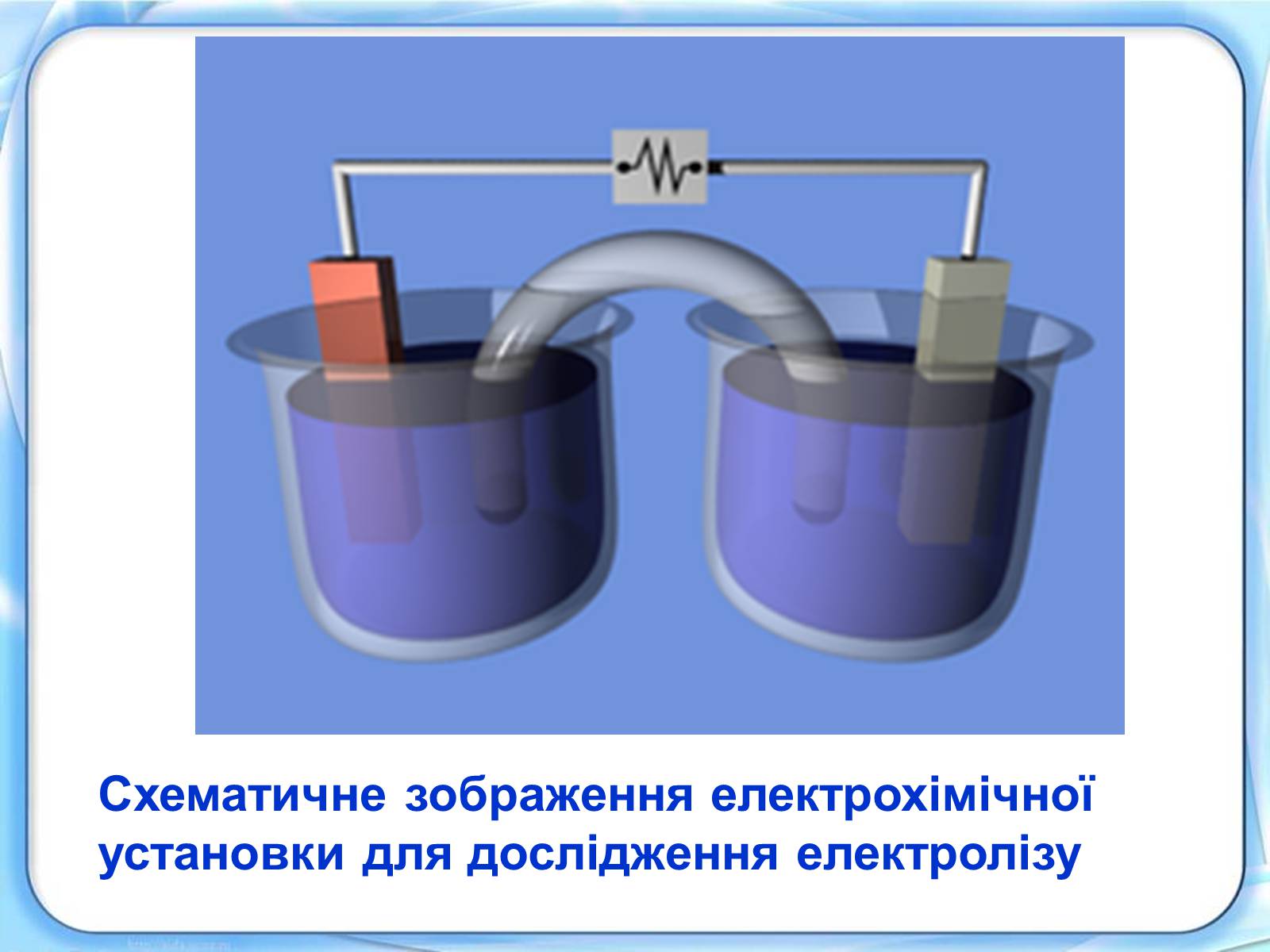
Схематичне зображення електрохімічної установки для дослідження електролізу
Слайд #7
Кількість іонів N дорівнює кількості атомів речовини, що виділиться на електроді, а маса виділеної речовини
де mo - маса одного атома, μ - молярна маса речовини.
де mo - маса одного атома, μ - молярна маса речовини.

Слайд #8
Електрохімічний еквівалент речовини
m = kq = kIΔt
Маса речовини, яка виділяється на катоді за час Δt, пропорційна силі струму і часу. Це твердження, встановлене експериментально Фарадеєм (1831 р.), має назву першого закону Фарадея для електролізу.
m = kq = kIΔt
Маса речовини, яка виділяється на катоді за час Δt, пропорційна силі струму і часу. Це твердження, встановлене експериментально Фарадеєм (1831 р.), має назву першого закону Фарадея для електролізу.

Слайд #9
Електрохімічний еквівалент речовини
m = kq = kIΔt
Маса речовини, яка виділяється на катоді за час Δt, пропорційна силі струму і часу. Це твердження, встановлене експериментально Фарадеєм (1831 р.), має назву першого закону Фарадея для електролізу.
m = kq = kIΔt
Маса речовини, яка виділяється на катоді за час Δt, пропорційна силі струму і часу. Це твердження, встановлене експериментально Фарадеєм (1831 р.), має назву першого закону Фарадея для електролізу.
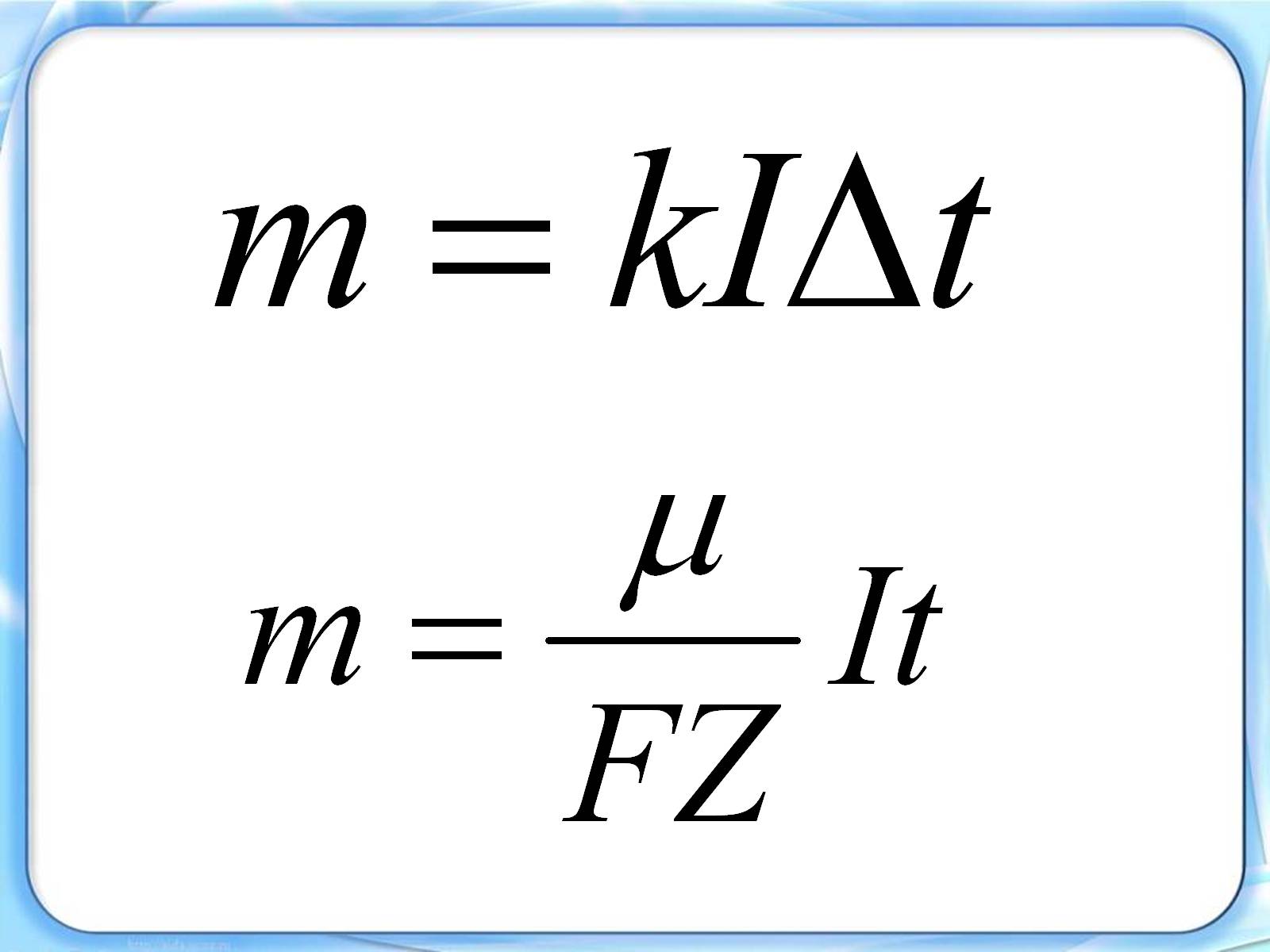
Слайд #10
Явище електролізу має широке застосування в електрометалургії (добування чистих металів); у гальваностегії (нанесення металевих покриттів для запобігання корозії металів); у гальванопластиці (виготовлення копій з матриць) тощо. Будову хімічних джерел струму (гальванічних елементів та акумуляторів) також засновано на процесах взаємодії металів з електролітами.

Слайд #11
Підготував
Учень 9-А класу –
Максьома Микола
Учень 9-А класу –
Максьома Микола
